【研究进展】我室陈瑶生教授团队联合四川农业大学李明洲教授团队、西北农林科技大学吴江维教授团队合作绘制猪肝脏高分辨率三维基因组动态图谱
肝脏是哺乳动物重要的免疫和代谢器官。猪作为重要的农业动物,因其饮食结构、生理特性和器官大小与人相似,有望成为重要的医学模型和人类肝脏移植的理想供体。
我室陈瑶生教授团队展开合作研究,利用Hi-C技术重构了猪肝脏从胚胎38天开始到成年时高脂日粮诱导肥胖过程中染色质空间构象变化的动态图谱,为深入了解猪肝脏在生长发育和代谢应激过程中的功能变化,特别是基因组三维结构重塑介导的转录调控改变提供了重要基础数据。
团队对猪从出生前到成年,共6个关键发育阶段和高脂饮食诱导肥胖后的肝脏进行研究,通过多组学联合分析(Hi-C、ATAC-seq、ChIP-seq和RNA-seq)发现猪肝脏的染色质空间构象在出生前后差异明显,在生长发育过程中其经历了从疏松到紧实的逐步建立过程,具体表现为互作矩阵秩序性的增加(冯诺依曼熵值:从0.66到0.42)、染色质区室的重排(区室化强度:从51.06 到 99.10)、拓扑结构关联域(TAD)的重构(TAD的连通性:从0.27到0.28)和启动子-增强子互作改变。以上基因组三维结构的变化为肝脏从出生前主要参与造血,到出生及成年后主要参与代谢,这一快速的功能转变提供了表达调控的结构基础。特别是,对成年后高脂饮食诱导肥胖组的分析表明:尽管体重增加2.03倍、背膘厚增加2.45倍,但猪的各项代谢指标和染色质层级构象并未发生明显变化。这与人和啮齿类的研究结果不同(70%的超重人群和啮齿动物都患有肝代谢疾病)。物种间差异提示家猪在驯化和人工选择过程中可能已经对“糖尿病易感‘diabetogenic’ environments”环境(高能饮食,较少活动)产生了代谢适应,进而在慢性肥胖的发生过程中肝脏对代谢应激产生了较强的抵抗力。
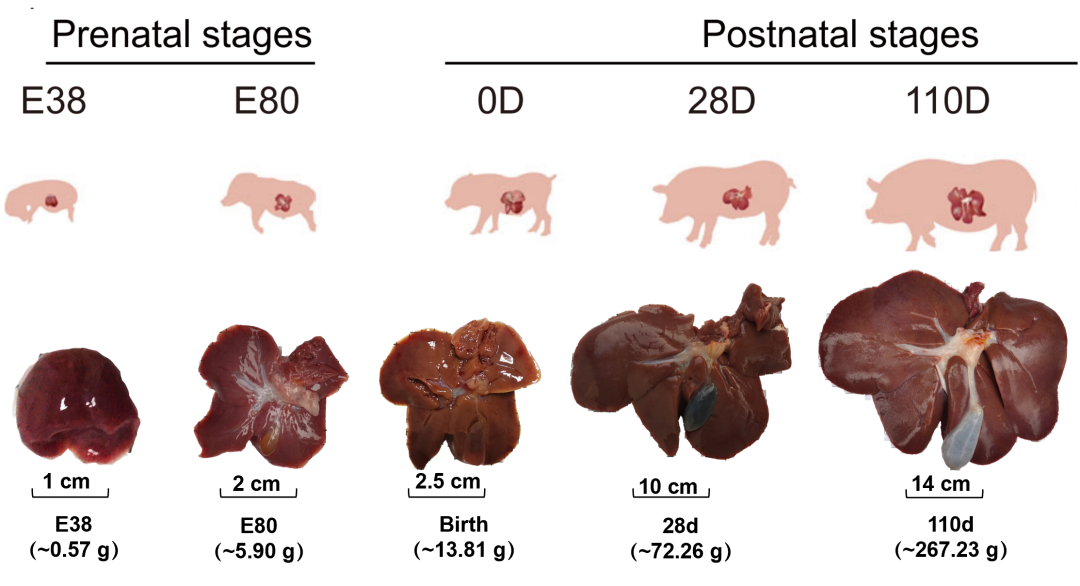
该研究成果“Dynamic 3D Genome Reorganization during Development and Metabolic Stress of the Porcine Liver(猪肝脏发育及代谢应激下的三维基因组动态图谱)”在Cell Discovery上发表。陈鹭曦博士、李晶博士、袁任强博士、博士研究生王誉杰、张佳满、林育为共同第一作者。我室陈瑶生教授、四川农业大学李明洲教授、西北农林科技大学吴江维教授为共同通讯作者。有害生物控制与资源利用国家重点实验室为第一完成单位。
专家点评
邓伍兰 研究员 (北京大学)
肝脏作为重要的代谢器官,解析其在发育和应激过程中基因表达调控的动态变化规律是理解其表型形成和相关致病机理的重要基础。近年来,基于荧光成像、4C及其衍生技术等多种实验手段,已认识到细胞核内染色质的三维空间构象对基因转录的重要调控作用。但目前,我们对哺乳动物肝脏发育和代谢应激过程中染色质空间构象的动态变化规律知之甚少。阐明这些问题,有助于加深我们对肝脏转录调控事件的完整认识。
近日,四川农业大学、中山大学和西北农林科技大学等国内多家单位合作发表于Cell Discovery的论文,以高深度in situ Hi-C为基础,结合组蛋白修饰和基因表达等多组学数据,绘制了家猪肝脏发育及代谢应激过程中的高分辨率三维基因组动态图谱。发现在肝脏发育早期,基因组呈现更松散、可及性更强的染色质构象,伴随着更广泛的转录事件,随后染色质高级结构如区室(Compartments)和拓扑关联域(TADs)等逐渐建立并不断加强。在整个生长发育过程中,染色质空间构象与启动子、增强子的组蛋白修饰活性和基因转录活性高度相关,表现为造血相关基因在发育早期位于更活跃的A区室,且具有更强的启动子-增强子互作(PEIs),其组蛋白修饰活性和转录水平亦更高,而与代谢和免疫相关基因则在生长发育后期才呈现这类特征。该研究还发现与正常体重的家猪肝脏相比,高脂饲喂诱导肥胖家猪的肝脏并未表现出明显的脂质代谢异常及染色质空间构象变化,提示家猪作为重要的肉用家畜,其在漫长的驯化和近期的人工选择过程中已产生对圈养环境下高脂高能日粮导致代谢应激的遗传适应性。该研究成果不仅加深了我们对染色质空间构象介导基因表达调控的动态规律的认识,也为深入理解家猪这一重要农业动物的代谢生理特点提供了重要数据。
李于 研究员(中科院上海营养与健康研究所)
猪拥有与人类非常相似的基因以及肥胖倾向性等多种特征,因而成为研究人类肥胖、糖尿病、心血管疾病等代谢性疾病理想模式动物及潜在的器官移植供体。肝脏是体内最大的物质代谢器官,其功能紊乱会导致各种疾病。染色质三维结构是重要的表观遗传因素,其动态改变影响肝脏基因表达调控,与肝脏发育及疾病发生发展密切相关。猪肝脏不同发育阶段及高脂饮食条件下染色质三维结构的变化规律尚未探索。
近期,四川农业大学李明洲教授团队、中山大学陈瑶生教授团队和西北农林科技大学吴江维教授团队合作,采用巴马小型猪动物模型,首次构建了不同发育阶段以及高脂诱导的肥胖猪的肝脏染色质三维结构图谱,追踪了猪肝脏组织的染色质空间构象重编程过程,明确了肝脏组织染色质结构重编程在机体发育及代谢调控中的关键作用。有意思的是,虽然高脂饮食显著增加猪体重和肝脏重量,但并不影响血糖、血脂、肝脂等代谢指标,表明猪能够抵抗饮食诱导的糖尿病与脂肪肝。本研究结果有助于解析能量摄入过度条件下猪与人不同的代谢适应性调控机制。该项研究还发现了肝脏发育和肝癌之间的部分相似性,通过Hi-C数据清晰阐释了异常基因的表达模式,阐明了基因组拓扑结构、染色质状态和基因表达之间的密切相关性。该项研究绘制的全基因组高分辨率互作图谱有助于解析肝脏发育与功能的遗传基础,同时为人类肝脏以及肥胖相关疾病的防治提供重要理论依据。
Prof. Fernando Alvarez (加拿大蒙特利尔大学CHU Sainte-Justine医院)
This study applied multidimensional approaches Hi-C, ChIP-seq, ATAC-seq and RNA-seq to investigate chromatin landscapes and gene expression profiles of porcine livers at six representative developmental stages and under high fat diet (HFD) stress. This integrated analysis provides a systemic overview of chromatin architecture dynamics associated with the transition of physiological liver functions from prenatal development to postnatal maturation. The study also reveals a unique feature that pigs are more resistant to HFD-induced obesity, hyperglycemia and fatty liver, which undoubtedly merits further investigation. Another intriguing point of the study is the similarity in gene expression between fetal liver and hepatocarcinoma. This is a crucial observation given its clinical significance. Overall, this is a great team effort and pioneer work, highly innovative and original. It provides a foundational resource allowing for future in-depth functional characterization.
原文链接:https://www.nature.com/articles/s41421-022-00416-z